研究方向

 围绕“肿瘤微环境中免疫细胞空间分布及其可调控性”这一问题,课题组干湿结合,开展了深入的多学科交叉研究,已独立自主开发多项关键技术:空间免疫技术,包括空间单细胞高通量基因编辑与筛选技术、空间T/BCR测序技术、空间微生物组测序技术等;人工智能算法,包括计算病理学大模型、基于空间转录组的细胞重构扩散模型等。体内外基因编辑技术,包括人类与小鼠系统原代T细胞编辑技术,基于造血干细胞移植的体内CROP-Seq技术,肝脏内巨噬细胞编辑技术等。
围绕“肿瘤微环境中免疫细胞空间分布及其可调控性”这一问题,课题组干湿结合,开展了深入的多学科交叉研究,已独立自主开发多项关键技术:空间免疫技术,包括空间单细胞高通量基因编辑与筛选技术、空间T/BCR测序技术、空间微生物组测序技术等;人工智能算法,包括计算病理学大模型、基于空间转录组的细胞重构扩散模型等。体内外基因编辑技术,包括人类与小鼠系统原代T细胞编辑技术,基于造血干细胞移植的体内CROP-Seq技术,肝脏内巨噬细胞编辑技术等。
空间多组学测序技术
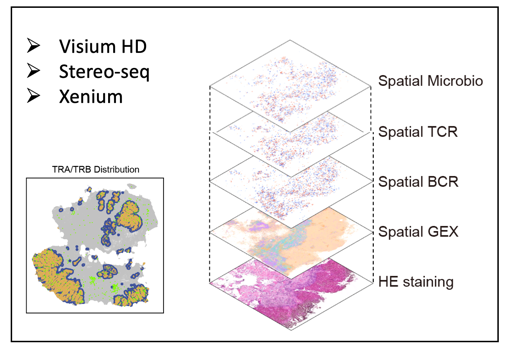
课题组基于Visium HD、Stereo-seq、Xenium等高通量、单细胞分辨率平台,开发了多种空间组学测序技术,涵盖空间微生物组测序、TCR/BCR测序等。并同步开发配套计算工具,对高维空间组学数据进行深度解析,实现肿瘤微环境的多维度解码。
CRISPR 库筛技术
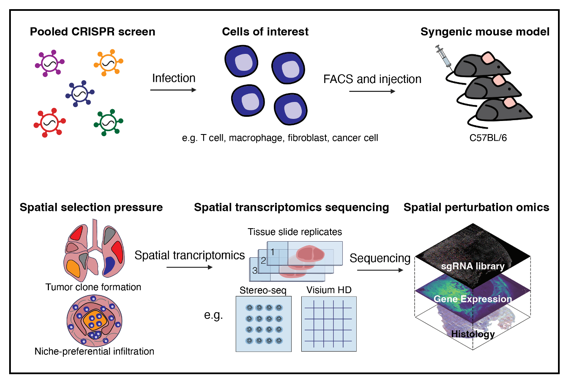
课题组开发了单细胞分辨率空间的CRISPR筛选技术,兼容了目前主流的空间转录组平台(如Stereo-seq、Visium HD)。此外,课题组设计针对多种免疫细胞和癌细胞的CRISPR筛选策略,包括CD4⁺ T细胞、CD8⁺ T细胞、B细胞、巨噬细胞和成纤维细胞,涵盖体外与体内模型,致力于揭示免疫过程的关键调控因子。
多组学人工智能模型
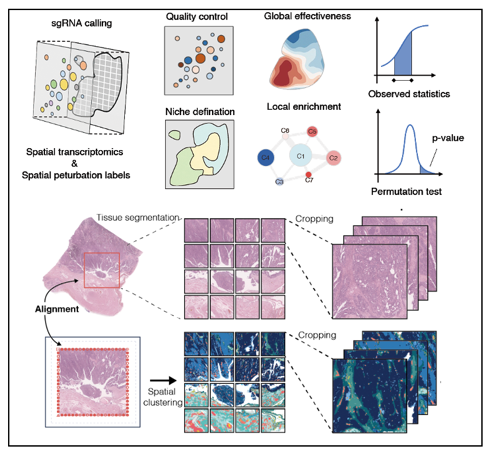
课题组开发机器学习与统计计算方法来分析复杂的多组学数据。开发的模型内容包括从零训练的基座大模型、微调现有模型以实现迁移学习。同时构建了基于Python与R的分析工具包,并开发交互式网页平台以实现数据的可视化与探索。课题组的目标是深入理解肿瘤微环境中多种生物因子的协同作用,并识别驱动免疫响应及疾病进展的关键调控基因。