免疫疗法在临床上取得了巨大成功,但大多数患者未能从治疗中获得持续的临床疗效。细胞毒性T细胞(CTL)是抗肿瘤免疫反应的关键效应细胞,它们通过T细胞受体(TCR)与肽-主要组织相容性复合物(MHC)的相互作用来特异性地识别肿瘤细胞。CTL会释放含有穿孔素和颗粒酶的细胞毒性颗粒以诱导靶细胞凋亡。因此,癌细胞通常会发展多种机制来避免CTL介导的识别和杀伤。其中,已知的机制包括抗原呈递途径的下调 [1,2],以及免疫抑制分子如PD-L1和SERPINB9的上调等 [3,4]。此外,CTL还释放TNFα 和IFNγ等细胞因子杀伤肿瘤细胞。然而,肿瘤细胞如何耐受细胞因子介导杀伤的分子机制尚不明确。
2023年7月27日,北京大学定量生物学中心(CQB)曾泽贤团队与清华大学医学院潘登团队,以及武汉大学中南医院汪付兵团队合作在Cell Metabolism上发表了题为 Tumor aerobic glycolysis confers immune evasion through modulating sensitivity to T cell-mediated bystander killing via TNFα 的研究论文,发现抑制肿瘤糖酵解和葡萄糖转运体1(Glut1)会增强 CTL对肿瘤细胞的杀伤。在机制方面,Glut1 失活会导致肿瘤氧化磷酸化水平(OXPHOS)上升,从而产生过量的活性氧化物(ROS),后者促进TNFα介导的细胞死亡。通过Glut1特异抑制剂BAY-876可使多种小鼠肿瘤细胞对抗肿瘤免疫更敏感。此外,由于CTL高表达另一个葡萄糖转运蛋白Glut3,抑制Glut1对CTL功能的影响相对较小。因此,靶向Glut1为肿瘤免疫疗法提供了新的治疗思路。

研究团队首先在小鼠肺癌细胞系LLC和胰腺癌细胞系Panc02中进行了全基因组的CRISPR-Cas9筛选以寻找抗CTL介导杀伤的基因。筛选发现,靶向糖酵解的关键基因如Slc2a1 (Glut1)、Gpi1、Pkm和Ldha 的sgRNA丰度显著下降,揭示了肿瘤细胞糖酵解通路在调控肿瘤抵抗CTL杀伤的关键作用。通过整合多套人类单细胞数据以及免疫荧光实验发现,Glut1在肿瘤细胞表达更高,而免疫细胞则选择性高表达Glut3用以摄取葡萄糖。因此研究团队选择Glut1作为潜在特异性靶向肿瘤细胞糖酵解通路的靶点继续深入研究。
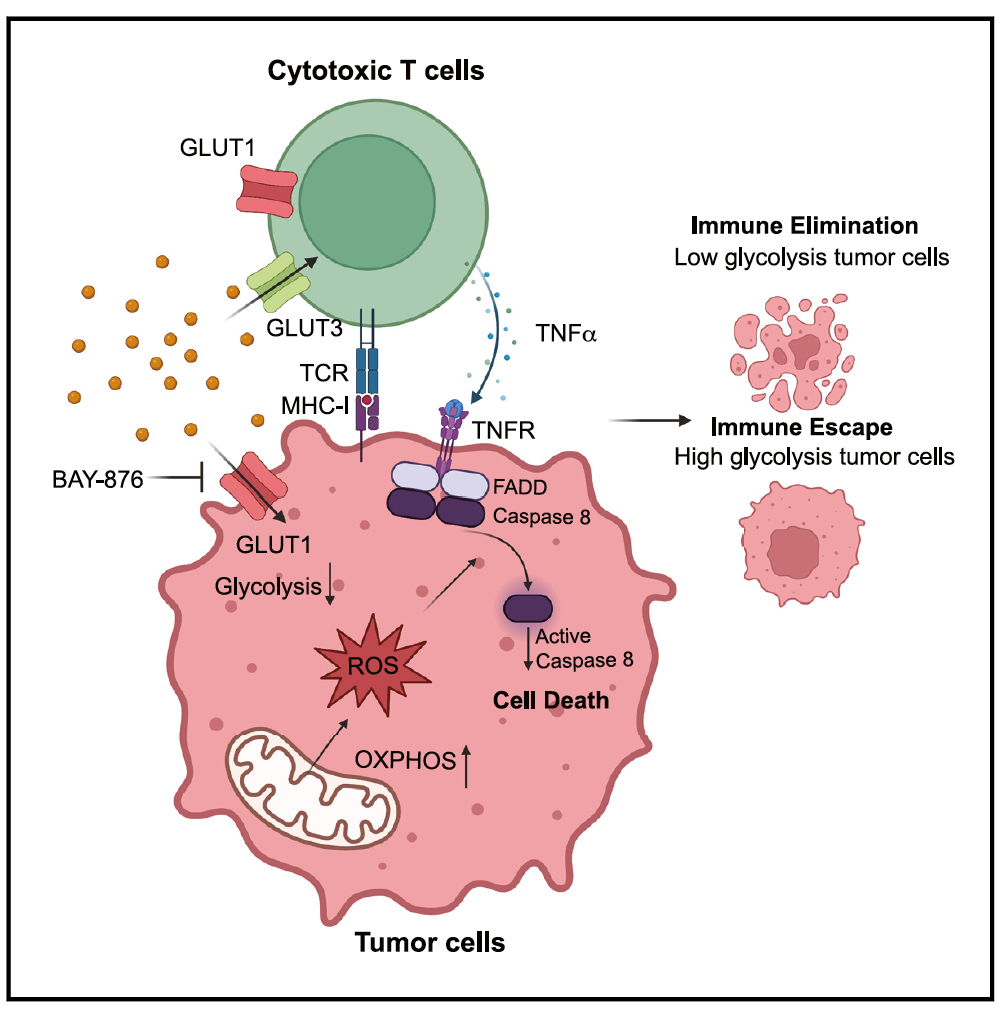
研究团队发现Glut1敲除所导致的对CTL杀伤敏感的表型不依赖肿瘤细胞与T细胞的直接接触,暗示了Glut1参与调控肿瘤细胞对CTL释放细胞因子杀伤的耐受。通过一系列生化和细胞实验,研究团队证明了Glut1缺失导致肿瘤细胞对TNFα 诱导的细胞死亡显著上升。在机理上, Glut1的抑制导致线粒体氧化磷酸化(OXPHOS)水平显著升高并产生大量的活性氧 (ROS),后者在细胞内的堆积导致c-Flip的水平下调,进而加剧TNFα诱导的细胞凋亡。
最后,在多种小鼠肿瘤模型中,研究团队发现抑制Glut1对于肿瘤在免疫缺陷小鼠中生长没有影响,却可以抑制肿瘤在免疫健全小鼠中的生长,表明靶向Glut1对肿瘤的抑制作用依赖于宿主的适应性免疫系统。重要的是,当使用TNFa受体敲除的肿瘤细胞时,抑制Glut1导致的肿瘤生长减缓的效应相应的消失,再次表明Glut1抑制与肿瘤TNFa通路密切相关。研究团队进一步分析了接受免疫检查点阻断(ICB)治疗的病人的临床试验数据集和TCGA数据库,发现糖酵解/Glut1特征的低表达与对ICB 更好的响应有关。
综上,研究团队报道了肿瘤细胞糖酵解参与调控CTL分泌TNFα介导杀伤的一种新机制,并发现Glut1为肿瘤细胞偏好性的糖酵解靶点,为提高现有疗法的响应率和开发新型免疫疗法提供了新的见解。
原文链接:https://doi.org/10.1016/j.cmet.2023.07.001
参考文献
Zaretsky, J. M. et al. Mutations Associated with Acquired Resistance to PD-1 Blockade in Melanoma. N Engl J Med 375, 819-829 (2016). https://doi.org:10.1056/NEJMoa16049582
Sade-Feldman, M. et al. Resistance to checkpoint blockade therapy through inactivation of antigen presentation. Nat Commun 8, 1136 (2017). https://doi.org:10.1038/s41467-017-01062-w3
Jiang, P. et al. Signatures of T cell dysfunction and exclusion predict cancer immunotherapy response. Nat Med 24, 1550-1558 (2018). https://doi.org:10.1038/s41591-018-0136-14
Juneja, V. R. et al. PD-L1 on tumor cells is sufficient for immune evasion in immunogenic tumors and inhibits CD8 T cell cytotoxicity. J Exp Med 214, 895-904 (2017). https://doi.org:10.1084/jem.20160801