衰老是机体功能衰退及多种慢性疾病的重要基础过程,细胞衰老则是驱动组织损伤和纤维化等病理改变的关键环节。与此同时,DNA损伤修复能力下降又是诱导细胞衰老的重要源头之一。相比蛋白编码基因,长链非编码RNA(lncRNA)在衰老中的系统性功能和分子机制仍不清楚。系统鉴定衰老相关lncRNA并解析其调控网络,对于深化衰老机制认识和寻找潜在干预靶点具有重要意义。
北京时间2026年3月31日,北京大学定量生物学中心韩敬东组在Nature Aging上发表了题为“Multiomic single-cell perturbation screens reveal critical lncRNA regulators of senescence”的研究论文。该文章利用单细胞多组学扰动筛选策略,系统构建了衰老相关长链非编码RNA(lncRNA)的多组学调控网络,并揭示了关键DNA修复相关lncRNA调控细胞衰老的分子机制及其潜在抗衰老干预价值。

研究团队首先整合多套公开衰老和细胞衰老相关转录组数据,筛选出32个高丰度、具有独立启动子、与衰老及细胞衰老显著相关的候选lncRNA,并将其定义为PtbAlncs。在此基础上,团队建立了结合CRISPRi扰动与单细胞多组学测序(10x Multiome)的“Perturb-Multiome”研究框架,在单细胞层面同时读出lncRNA扰动后的基因表达变化和染色质可及性变化,从而实现对转录层和表观遗传层的联合分析。
通过该平台在不同细胞系中的系统筛选,研究人员发现,多种PtbAlnc扰动都会引起与衰老密切相关的转录和染色质开放变化,其差异基因和差异开放染色质区域显著富集于细胞衰老、DNA损伤应答、p53信号、炎症反应及长寿调控等通路。进一步在BJ成纤维细胞中结合不同组学的单细胞衰老评分工具,研究团队识别出一批具有明确促衰老或抗衰老效应的lncRNA。例如,MIR155HG、NEAT1等lncRNA表现出抑制细胞衰老的效应,而HOTAIRM1缺失则显著促进细胞衰老。这些结果随后又在肺成纤维细胞WI-38中的SA-β-gal染色实验中得到了进一步验证。
在前述基础上,研究团队进一步分析了PtbAlnc扰动后单细胞中的RNA模块和ATAC模块,并建立了二者之间的整合对应关系。研究团队基于因果推断分析构建了PtbAlnc扰动—ATAC功能motif—RNA模块的三级因果调控网络,结果显示,不同PtbAlnc可通过scATAC-seq模块中多样但部分重叠的表观遗传motif,选择性调控不同的scRNA-seq转录模块。其中,HOTAIRM1是这一网络中的核心枢纽分子之一,主要通过BANF1、ARID1B和RB1等染色质调控相关motif,影响多个关键衰老相关转录模块。这一结果系统地在单细胞层面将lncRNA扰动、表观遗传状态变化和衰老相关表达程序联系起来。此外,在与衰老相关疾病的SNP富集分析中,PtbAlncs在肺组织相关衰老疾病中表现出最显著的富集信号。
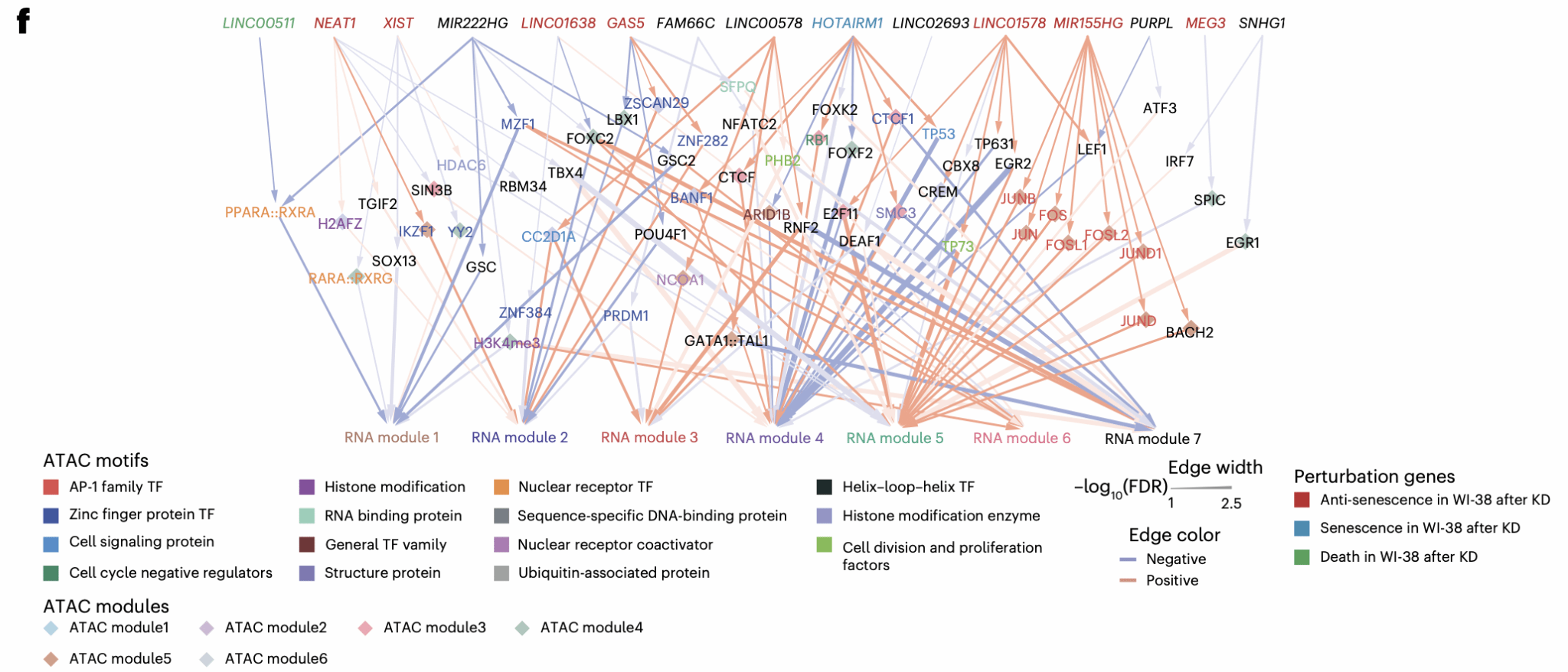
lncRNA—ATAC motif—RNA模块因果调控网络。不同PtbAlncs通过部分重叠的表观ATAC motif影响衰老相关转录程序。
在上述网络分析基础上,研究团队进一步聚焦代表性PtbAlnc—HOTAIRM1。RNA多组学整合分析显示,HOTAIRM1与DNA损伤修复及p53介导的衰老程序密切相关。进一步机制研究表明,HOTAIRM1可与BANF1和p53相互作用,在DNA双链断裂位点促进DNA修复相关过程的动态维持。HOTAIRM1缺失会削弱DNA修复效率,激活p53信号并诱导细胞衰老。此外,HOTAIRM1、BANF1和p53在体外还可形成凝聚体样结构,提示HOTAIRM1可能通过参与修复相关凝聚体的形成与维持,调控DNA损伤修复稳态。

HOTAIRM1协调DNA修复并调控p53介导的细胞衰老
在体内实验中,研究人员进一步发现,在自然衰老小鼠(20个月龄)中,AAV6介导的肺部靶向HOTAIRM1过表达可明显改善肺组织衰老表型,包括减轻纤维化、降低炎症和组织损伤、提高细胞增殖水平,并改善肺泡结构完整性,提示其具有潜在的抗衰老干预价值。
该研究建立了一套面向衰老相关lncRNA研究的单细胞多组学解析范式,不仅深化了对lncRNA调控衰老机制的认识,也为衰老相关疾病的干预提供了新的潜在靶点。
北京大学定量生物学中心/生命科学联合中心韩敬东教授为该论文的通讯作者。北京大学PTN项目博士研究生朱寿轩与北京大学博雅博士后营孙阳为该论文的共同第一作者。该项研究得到了国家自然科学基金以及北京大学-清华大学生命科学联合中心(CLS)等多项基金项目的支持与资助。
文章链接:https://www.nature.com/articles/s43587-026-01100-7